خبرهای فارسی
اخبار موسیقی، اخبار آی تی، اخبار ورزشی، اخبار استخدامخبرهای فارسی
اخبار موسیقی، اخبار آی تی، اخبار ورزشی، اخبار استخدامتاریخچه شیمی
تاریخچه شیمی
واژه شیمی خود داستان درازی دارد. ریشه این نام در واژه کیمیاست. خاستگاه واژه کیمیا از زبان فارسی باستان است. این واژه و داستان دانش شگفت انگیز پشت آن به همراه دانشش به زبان عربی نوشته شد و اروپاییان با این واژه و دانش آن از راه مسلمانان آشنا شدند و این دانش را با نام alchemy شناختند. آنگاه آن را در میان خود پروردند تا در سدههای نزدیک به ریخت فرانسه شیمی به زبان ما بازگشت. دانش شیمی به دو گرایش شیمی محض و شیمی کاربردی تقسیم میشود.علم شیمی از ابتدا تا کنون به ۵ دوران تقسیم میشود ۱.دوران رشد کارهای تجربی ۲.دوران رشد جنبههای تئوری شیمی ۳.دوران کیمیا گری ۴.دوران اصل اتش ۵.دوران شیمی مدرن
شیمی یکی از علومی است که هموراه در زندگی بشر دخالت کامل داشته و وارد و به اندازه که تمدن کنونی بیشتر شود دخالت آن در شئون مختلف زندگی نیز زیادتر خواهد شد. ما در دنیایی زندگی می کنیم که پر از مواد شیمیایی گوناگون است. بعضی از این مواد مانند آب کاملاً برایمان آشنا است اما بسیاری مواد دیگر وجود دارند که چندان آشنا نیستند. واقعیت آن است که ما از هر لحاظ با مواد شیمیایی روبرو هستیم. لباسی که می پوشیم، غذایی که مصرف می کنیم، کاغذی که مطالب را روی آن می خوانیم همگی مواد شیمیایی به شمار می روند. علم شیمی از اجسام و خواص و ساختمان آنها و واکنشهایی که آنها را به اجسام دیگر تبدیل می نماید بحث می کند. طی هزاران سال، دانش شیمی تنها منحصر به تهیه اکسیرها، عطرها و جوهر های پاره ای از فلزات بود. یونانیان قرن پنجم که همواره در صدد پی بردن به رموز و اسرار طبیعت بودند آب را که مایه حیات سایر موجودات است عنصری ساده می پنداشتند حال آنکه آب ترکیبی از دو عنصر ساده اکسیژن و هیدروژن است.
فکر اولیه وجود عناصر ساده ابتدا از امپدوکل و سپس از ارسطو می باشد. ارسطو معتقد بود که چهار عنصر آب، هوا، خاک و آتش مظهر خواص اصلی از قبیل رنگ، استحکام و حالت اجسام می باشند و از ترکیب آنها مواد گوناگون به وجود می آید.
شیمی در طول تاریخ طولانی و تکاملی خود دورانهای گوناگونی را پشت سر گذاشته که می توان آن را به سه بخش عمده تقسیم کرد: دوران باستان که هنوز شیمی به صورت یک علم مشخص درنیامده بود. دوران کیمیاگری از آستانه پیدایش مسیحیت تا سالهای 1700 میلادی و دوران شیمی جدید.
در سراسر دوران تاریک قرون وسطی دانش شیمی نیز همچون دیگر رشته های علوم پیشرفت قابل ملاحظه ای ننمود. کشف الکل و جوهر گوگرد به وسیله کیمیاگر ایرانی محمد زکریای رازی و کشف فسفر در سال 1675 میلادی توسط براند آلمانی از آثار دوره کیمیاگری است. کیمیاگری تنها در اواخر قرن هفدهم و اوایل قرن هجدهم بود که به صورت دانشی حقیقی و واقعی به نام شیمی در آمد. رابرت بویل انگلیسی نخستین کسی بود که دلیرانه با نظرات و عقاید قدما درباره وجود عناصر چهارگانه و تبدیل فلزات مخالفت نمود. به عقیده بویل عنصر جسمی است غیرقابل تجزیه و از ترکیب آنها اجسام مختلف پدید می آید. نظریات بویل در کتاب شیمیدانان شکاک کم و بیش یادآور نگرش ابن سینا در کتاب «ابطال کیمیا» است که در شش قرن پیش از آن به رشته تحریر درآورد. ژوزف بلاک شیمیست اسکاتلندی در سال 1757 گاز کربنیک را به دست آورد و آن را هوای ثابت نامید. ژوزف پریستلی انگلیسی در سال 1774 گاز اکسیژن را ضمن حرارت دادن اکسید قرمز جیوه برای نخستین بار تهیه کرد. هنری کاواندیش دانشمند انگلیسی نیز در سال 1766 هیدروژن خالص را کشف نمود و خواص آن را معلوم و مشخص نمود. برگمان شیمیست سوئدی این نظر را ارائه کرد که هوا مخلوطی از سه گاز است. هوای معیوب (ازت)، هوای خالص (اکسیژن) و اسید هوایی (گاز کربنیک) بالاخره شارک گیوم سئل شیمیست دیگر سوئدی درباره بی اکسید منگنز مطالعاتی کرد و همین موضوع راهنمای او برای تهیه اکسیژن گردید. لاووازیه که در حقیقت بنیانگذار شیمی جدید محسوب می شود گامهای بلندی در راه آزمایش و پژوهش علمی برداشت. کشف گازهای اکسیژن و هیدروژن به لاووازیه این امکان را داد که به تفسیر علمی درستی برای پدیده سوخت و ارتباط آن با هوا نائل آید. لاووازیه ثابت نمود که عمل سوختن ترکیب جسم است با اکسیژن و در این مورد یکی از قوانین اصلی شیمی یعنی اصل بقاء ماده را به شرح زیر وضع کرد:
هیچ چیز از بین نمی رود و هیچ چیز خلق نمی شود. در تمام واکنشهای شیمیایی مجموع وزنهای مواد پیش از فعل و انفعال شیمیایی مساوی وزنهای مواد به دست آمده است.
در آغاز قرن هجدهم یعنی در سال 1800 میلادی ولتا فیزیکدان انگلیسی نخستین پیل را کشف کرد و از آن پس الکتروشیمی در دسترس جهانیان قرار گرفت. دیوی انگلیسی از تجزیه الکتریکی پتاس مذاب فلز پتاسیم و سپس از سود گداخته فلز سدیم را به دست آورد. او با تجزیه الکتریکی ثابت کرد که برخلاف عقیده لاووازیه که اکسیژن را عامل ترشی می نامید تمام اسیدها اکسیژن ندارند. همچنین وهلر آلمانی در آغاز این قرن با استفاده از پتاسیم موفق به کشف آلومینیوم گردید و از آن پس عناصر یکی پس از دیگری پیدا شدند. در اواخر نوزدهم دیمتری مندلیف شیمیست نابغه روس با تنظیم جدول تناوبی معروف خود عده زیادی از عناصر را از خاصیت تکرار اتمها پیش بینی کرد و با کشف آنها شیمی در ردیف علوم مدرن و درجه اول قرار گرفت. بالاخره در حدود سال 1760 برتلو شیمیست بزرگ فرانسوی توانست از ترکیب مستقیم کربن و هیدروژن استیلن را تهیه نماید. شیمی جدید به عنوان یک علم نظام یافت طی 200 سال گذشته شکل گرفت و از همان آغاز به کلی از شیوه های کیمیاگری دور شد. از آغازقرن نوزدهم تا کشف و نوآوری در علم شیمی و کاربردهای آن در تکنولوژی و زندگی با سرعت هرچه تمامتر ادامه دارد.
نگاه گذرا
تئوری اتمی پایه و اساس علم شیمی است. این تئوری بیان میدارد که تمام مواد از واحدهای بسیار کوچکی به نام اتم تشکیل شدهاند. یکی از اصول و قوانینی که در مطرح شدن شیمی به عنوان یک علم تأثیر بهسزایی داشته، اصل بقای جرم است. این قانون بیان میکند که در طول انجام یک واکنش شیمیایی معمولی، مقدار ماده تغییر نمیکند. (امروزه فیزیک مدرن ثابت کرده که در واقع این انرژی است که بدون تغییر میماند و همچنین انرژی و جرم با یکدیگر رابطه دارند.)
این مطلب به طور ساده به این معنی است که اگر دههزار اتم داشته باشیم و مقدار زیادی واکنش شیمیایی انجام پذیرد، در پایان ما همچنان بطور دقیق دههزار اتم خواهیم داشت. اگر انرژی از دست رفته یا بهدستآمده را مد نظر قرار دهیم، مقدار جرم نیز تغییر نمیکند. شیمی کنش و واکنش میان اتمها را به تنهایی یا در بیشتر موارد بههمراه دیگر اتمها و بهصورت یون یا مولکول (ترکیب) بررسی میکند.
این اتمها اغلب با اتمهای دیگر واکنشهایی را انجام میدهند. (برای نمونه زمانیکه آتش چوب را میسوزاند واکنشی است بین اتمهای اکسیژن موجود در هوا که نور بر روی مواد شیمیایی فیلم عکاسی ایجاد میکند شکل میگیرد.)
یکی از یافتههای بنیادین و جالب دانش شیمی این بودهاست که اتمها رویهمرفته همیشه به نسبت برابر با یکدیگر ترکیب میشوند. سیلیس دارای ساختمانی است که نسبت اتمهای سیلیسیوم به اکسیژن در آن یک به دو است. امروزه ثابت شدهاست که استثناهایی در زمینهٔ قانون نسبتهای معین وجود دارد(مواد غیر استوکیومتری).
یکی دیگر از یافتههای کلیدی شیمی این بود که زمانی که یک واکنش شیمیایی مشخص رخ میدهد، مقدار انرژی که بدست میآید یا از دست میرود همواره یکسان است. این امر ما را به مفاهیم مهمی مانند تعادل ، ترمودینامیک میرساند.
شیمی فیزیک بر پایهٔ فیزیک پیشرفته (مدرن) بنا شدهاست. اصولاً میتوان تمام سیستمهای شیمیایی را با استفاده از تئوری مکانیک کوانتوم شرح داد. این تئوری از لحاظ ریاضی پیچیده بوده و عمیقاً شهودی است. به هر حال در عمل و بطور واقعی تنها بررسی سیستمهای سادهٔ شیمیایی قابل بررسی با مفاهیم مکانیکی کوانتوم امکانپذیر است و در اکثر مواقع باید از تقریب استفاده کرد(مانند تئوری کاری دانسیته). بنابراین درک کامل مکانیک کوانتوم برای تمامی مباحث شیمی کاربرد ندارد؛ زیرا نتایج مهم این تئوری (بخصوص اربیتال اتمی) با استفاده از مفاهیم سادهتری قابل درک و بهکارگیری هستند.
با اینکه در بسیاری موارد ممکن است مکانیک کوانتوم نادیده گرفته شود، مفهوم اساسی که پشت آن است، یعنی کوانتومی کردن انرژی، چنین نیست. شیمیدانها برای بکارگیری کلیه روشهای طیف نمایی به آثار و نتایج کوانتوم وابستهاند، هرچند که ممکن است بسیاری از آنها از این امر آگاه نباشند. علم فیزیک هم ممکن است مورد بی توجهی واقع شود، اما به هر حال برآیند نهایی آن (مانند رزونانس مغناطیسی هستهای) پژوهیده و مطالعه میشود.
یکی دیگر از تئوریهای اصلی فیزیک مدرن که نباید نادیده گرفته شود نظریه نسبیت است. این نظریه که از دیدگاه ریاضی پیچیدهاست، شرح کامل فیزیکی علم شیمی است. مفاهیم نسبیتی تنها در برخی از محاسبات خیلی دقیق ساختمان هسته، بهویژه در عناصر سنگینتر، کاربرد دارند و در عمل تقریباً با شیمی پیوند ندارند.
بخشهای اصلی دانش شیمی عبارتاند از:
شیمی تجزیه، که به تعیین ترکیبات مواد و اجزای تشکیل دهنده آنها میپردازد.
شیمی آلی، که به مطالعهٔ ترکیبات کربندار، غیر از ترکیباتی چون دو اکسید کربن (دی اکسید کربن) میپردازد.
شیمی معدنی، که به اکثریت عناصری که در شیمی آلی روی آنها تاکید نشده و برخی خواص مولکولها میپردازد.
شیمی فیزیک، که پایه و اساس کلیهٔ شاخههای دیگر را تشکیل میدهد، و شامل ویژگیهای فیزیکی مواد و ابزار تئوری بررسی آنهاست.
دیگر رشتههای مطالعاتی و شاخههای تخصصی که با شیمی پیوند دارند عبارتاند از: علم مواد، مهندسی شیمی، شیمی بسپار، شیمی محیط زیست و داروسازی.
شاخههای شیمی
شیمی آلی - شیمی معدنی - شیمی تجریه- شیمی فیزیک - شیمی گاز - نانو طراحی فرآیندهای صنایع نفت - فیتو شیمی - شیمی کاربردی - شیمی پالایش - زیستشیمی (بیوشیمی) - شیمی محض - شیمی دریا - شیمی آموزش
کلمهٔ کیمیا از کلمها ی فارسی بوده و به معنای طلا میباشد.و به خاطر قدمت این علم در ایران ان را علم بومی ایران دانستهاند.
عنصر شیمیایی
عنصر شیمیایی، در دانش شیمی، به مادهای گفته میشود که اتمهای آن تعداد پروتونهای برابر در هستهی خود داشته باشند. گاهی نیز برای سادگی، به عنصر شیمیایی صرفاً عنصر گفته میشود. به تعداد پروتونهای درون هستهٔ یک اتم، عدد اتمی گفته میشود. به عنوان مثال، تمام اتمهایی که ۶ عدد پروتون در هستهٔ خود داشته باشند، عنصر شیمیایی کربن هستند. همچنین تمام اتمهایی که تعداد پروتونهای درون هستهٔ آنها ۹۲ عدد باشد، عنصر اورانیوم به شمار میروند. هم اکنون تعداد عناصر شیمیایی در جدول تناوبی حدود ۱۱۵ عنصر برآورد میشود.
مولکول
مولکول، کوچکترین ذره یک ماده شیمیایی خالص است که ویژگیهای آن ماده را دارد. یک مولکول از دو یا چند اتم تشکیل شده که با پیوند شیمیایی به هم متصلند. البته مولکول بعضی عناصر (همچون گازهای بیاثر) تنها از یک اتم تشکیل شده است.
اتمهای تشکیل دهنده یک مولکول، ممکن است از یک عنصر (به طور مثال در اکسیژن) یا چند عنصر (مثلاً در آب) تشکیل شده باشند.
نسبت اتمها در یک مولکول خاص همیشه ثابت است. برای مثال در مولکول آب نسبت اتمهای هیدروژن به اکسیژن همیشه 2 است. تعداد اتمهای موجود در یک مولکول به وسیله فرمول شیمیایی آن نشان داده میشود. البته باید توجه داشت که تنها فرمول شیمیایی نشان دهنده ویژگیهای ماده نیست. ممکن است دو ماده فرمول شیمیایی یکسانی داشته باشند، اما ویژگیهای آنها کاملاً متفاوت باشد. برای مثال اتانول و دیمتیل اتر فرمول شیمیایی یکسان، اما خواص شیمیایی متفاوت دارند. به این مواد ایزومر گفته میشود.
مولکول
یک مولکول ، مجموعه ای از اتم های یک ماده ی مشخص دارای فرمول شیمیایی است. کلمه مولکول از زبان لاتین گرفته شده وبه معنی یک توده ی کوچکی از مواد می باشد برای مثال مولکول متان(CH4) از یک اتم کربن و چهار اتم هیدروژن تشکیل شده است.
یک مولکول ذره ای از موادی است که دارای قابلیت حرکت و مستعد دادن واکنش شیمیایی با مواد دیگرهستند در حالی که اتم از ذرات کوچک ثابت تری تشکیل شده و جابجای انها نیازمند انرژی بسیار زیادی است که برای انجام واکنش های هسته ای ضروری است
خاصیت مولکولها
مولکول های یک ماده در حال جنبش و حرکت دایمی هستند این جنبش مولکول ها حرکت براون نام دارد که برای اولین بار توسط روبرت براون در سال 1821میلادی کشف شده است. وقتی ماده به شکل گاز است مولکول ها دارای جنبش بسیار زیاد هستند و فضای ما بین مولکولها زیاد است در حالت مایع فضای بین مولکولی کمتر و جنبش مولکول ها نیز کمتر است در حالت جامد مولکولها به صورت منظمی چیده شدند و دارای چرخش به دور یک فضای مشخص هستند دمای یک ماده نشانگر میزان جنبش مولکول های آن ماده است
نیروی واندروالس یک نیروی ضعیفی است که بیانگرفاصله ی بین مولکول هاست .
ماکرومولکول ها
مولکولهای که دارای اندازه ی خیلی بزرگ هستند و حداقل از چندین هزار اتم تشکیل شدند : مثل پروتئینها , اسید های نوکلئیک و کربوهیدراتها
ترکیبات غیر مولکولی
شامل دو دسته ی بزرگ هستند ; فلزات و ترکیبات یونی
فلزات که از دسته ای از اتم های مرتبط با هم تشکیل شده و دارای پیوند فلزی میباشد
ترکیبات یونی مجموعه ای از اتم های دارای پیوند های یونی می باشند.
شیمی و آلودگی محیط زیست
شیمی در محیط زیست ما نقش اساسی دارد. در واقع در بین مردم متداول است که بیشتر مسائل آلودگی جاری را به گردن مواد شیمیایی سنتزی و پدید آورندگان آنها بیاندازند. اما این نکته ناگفته میماند که بیشتر مسائل زیست محیطی ، قرنها و دهههای گذشته ، مانند آلودگی میکروبی آب آشامیدنی ، تنها زمانی برطرف شدند که روشهای علمی بطور کلی و شیمی بطور اخص در مورد آنها بکار گرفته شد. افزایش شگفت انگیز عمر انسان و بهبود کیفیت زندگی در دهههای اخیر به مقدار زیاد به علت پیشرفت شیمی و پدید آمدن مواد شیمیایی جدید بوده است.
محصولات فرعی اجسامی که برای بهتر شدن سلامتی و بالا رفتن استاندارد زندگی ما بکار گرفته شدهاند، در مواردی بوسیله تنزل دادن سلامتی ما و همچنین سلامتی گیاهان و حیوانات ، همچون شبهی ما را دنبال میکنند. بطور خلاصه ، غلبه ما بر آلودگی گسترده زیست شناختی و بالا بردن استانداردهای سلامتی و ثروت مادی در کشورهای توسعه یافته به قیمت آلودگی شیمیایی گسترده کره زمین در سطح کم تمام شده است.
مواد شیمیایی و نظرات دانشمندان
تا به حال در بین دانشمندان در این باره که آیا آلودگی بوسیله مواد شیمیایی در سطح کم بر روی سلامتی انسانها یا سایر موجودات زنده اثر مضر و نامطلوب دارد، اتفاق نظر نیست. بعضی از دانشمندان ، خطر هر گونه اثرهای زیان آوری را به علت تاثیر مواد شیمیایی سنتزی (بویژه موادی که در ایجاد سرطان دخالت دارند) بطور کامل رد میکنند. این مواد به غلظتهای خیلی بیشتر اجسام سمی طبیعی مانند آفت کشهایی که بوسیله گیاهان تولید میشود و ما در معرض آنها قرار داریم، اشاره میکنند. در انتهای دیگر این طیف ، دانشمندانی هستند که معتقدند مواد شیمیایی در محیط زیست نقش عمدهای در شروع انواع معینی از سرطانها و نواقص در انسانها و حیات وحش دارند
راههای جلوگیری از آلودگی
این نکته روشن است که احتمالا سلامتی و رفاه انسانها از راههای ظریف اما موثری بوسیله غلظتهای کم از مواد شیمیایی در محیط زیست ما تحت تاثیر قرار میگیرد. از نظر تاریخی بطور ضمنی یا به طور صریح اینطور فرض شده بود که مواد شیمیایی منتشر شده در محیط زیست بوسیله طبیعت تحلیل خواهند رفت. اما امروزه میدانیم که چنین نیست. بسیاری از مواد پلیمری که امروزه در جامعه و صنعت تولید میشوند قرنها قابل تجزیه و بازگشت به چرخه طبیعی نیستند.
راهبرد اولیه این بود اغلب بوسیله جمع آوری و دور ریختن تودههای زیادی از این مواد ، پیش از اینکه در محیط زیست پخش شوند، از رها شدن آنها جلوگیری شود. پس از جمع آوری ، آنها را به صورت اجسام جامد درمیآورند و در زمینهای بایر میریزند. یک اشکال این قبیل راهبردها این است که آلایندهها معمولا در این فرآیند منهدم نمیشوند بلکه صرفا به صورت مطلوبتری درمیآیند یا اینکه در محیط متفاوتی رسوب داده میشوند. راهبرد شیمی سبز که اکنون جای راه حل بالا را میگیرد، تجدید نظر در فرمول بندی راههایی است که در سنتز مواد شیمیایی در درجه اول محصولات فرعی سمی تولید نشوند.
قلمروهای شیمی زیست
موضوع شیمی محیط زیست هم شامل اجسام و فرآیندهای طبیعی است که در یک محیط زیست پاکیزه حائز اهمیتند و هم اینکه مسائل آلودگی قابل ملاحظهای را که مبنای شیمیایی دارند، دربرمیگیرد. اگر چه طبیعت اکثرا موضوعهای مورد بحث به گونهای است که بیش از یک محیط فیزیکی یا یک ترکیب را دربرمیگیرند، اما مطالب مورد بحث شیمی محیط زیست به اینگونه طبقه بندی کلی میشوند:
شیمی اتمسفر
مواد شیمیایی آلی سمی - شیمی آب ، از جمله فلزات سنگین و نقش خاکها و رسوبها
منابع سوخت و انرژی ، از جمله انرژی هستهای - مسائل محیط زیستی بطور کلی ناشی از افزایش جمعیت دنیاست افزون بر این بسیاری از مسائل زیست محیطی وجود دارند که مورد بحث شیمی محیط زیست نیستند، زیرا این مسائل عمدتا منشا شیمیایی ندارند.
بخش سوم : تنظیم رطوبت و نگهداری نهایی در دستگاه جوجه کشی

قسمت سوم از مقاله دکتر تام دبلیو اسمیت آماده شده است .این مقاله نکات مهم جوجه کشی از انتخاب تخم تا خروج از تخم را به طور بررسی کرده و آموزش می دهد.اگر قسمت های قبلی این مقاله را مطالعه نفرموده اید پیشنهاد می کنیم قسمت اول آموزش حمل و نحوه مراقبت از تخم ها در جوجه کشی
و همچنین بخش دوم : انتخاب ماشین جوجه کشی مناسب را مطالعه فرمایید.
و اما بخش سوم
رطوبت بسیاربالا در تهویه کردن مناسب دستگاه جوجه کشی تأثیردارد. مساحت ظرف آب باید معادل نصف مساحت سطح کف یا بیشتر باشد. افزایش تهویه در طول چند روز مانده به جوجه کشی و جوجه ریزی ممکن است مستلزم ظرف دیگری از آب و یا یک اسفنج مرطوب باشد. رطوبت با افزایش سطح آب بدون پوشش حفظ می شود.
تهویه در طول فرایند جوجه کشی بسیار مهم است. در حالی که جنین در حال رشد است، اکسیژن وارد تخم مرغ از طریق پوسته و گریز دی اکسید کربن به همان صورت انجام می شود. از آنجا که تخم جوجه نیاز به یک منبع اکسیژن تازه دارد. همانطور که جنینها رشد می کنند، دهانه دریچه هوا به تدریج برای برآوردن افزایش تقاضا اکسیژن جنینی باز می شود. باید رطوبت در طول دوره جوجه کشی حفظ شود. سوراخ تهویه بدون مانع، هر دو، بالا و پایین تخم مرغ ها ، برای تبادل هوا مناسب ضروری است.
اگر در طول جوجه کشی دستگاه خاموش شود چه باید کرد ؟ پاسخ مناسب بستگی به عوامل متعدد دارد که عبارتند از درجه حرارت اتاق که دستگاه جوجه کشی در آن قرار گرفته است، تعداد تخم مرغ های در ماشین جوجه کشی و اینکه آیا تخم مرغ در مراحل اولیه و یا پایانی جوجه کشی قرار دارد.
در نظر گرفتن دو وضعیت مهم است (1) نگه داشتن بیش از حد تخم مرغ ها و (2) مطمئن شوید که آنها اکسیژن یکسان دریافت می کنند. در طول جوجه کشی بیشتر شدن تعداد تخم مرغ ها در ماشین جوجه کشی، شانس خفگی جنین ها را افزایش می دهد.
اگر اتاق که در آن ماشین جوجه کشی قرار گرفته است داغ باشد شما باید به سرعت اقدام کنید تا راه خروج هوا پیدا کند و اتاق در دمای مناسب بماند و به خوبی تهویه شود. موثر ترین مقابله برای جوش آوردن تخم باز کردن درب ماشین جوجه کشی یا محل تکثیر است اگر چه درب کمی و یا به طور کامل باز شود و مدت زمان آن گذشته باشد بستگی به عوامل که قبلا ذکر شده، دارد.
در مدت جوجه کشی تخم مرغ ها باید حداقل 4-6 بار در روز جابه جا شوند. تخم مرغ ها نباید سه روز قبل از در آمدن جوجه ها از تخم جابه جا شوند ( چرخش ). جنین ها موقعیت شکستن تخم خود را با جابه جایی از دست می دهند و نیازی به جابه جایی نیست. برای حفظ رطوبت و دمای مناسب درب دستگاه جوجه کشی را در مدت بیرون آمدن جوجه ها از تخم بسته نگه دارید. دریچه های هوا در مرحله بعدی از در آمدن جوجه ها از تخم باید به طور کامل باز باشند.
دستگاه غواصی
فن شناوری در زیر آب یا غواصی علاوه بر اینکه کاربردهای صنعتی، پژوهشی و نظامی دارد، ورزش و تفریحی لذتبخش نیز به شمار می رود. غواصی مثل تمامی حوزه ها در سالهای اخیر پیشرفتهای شایان توجهی داشته و لذا انتقال دانش و روشهای نوین غواصی به کشور ضرورتی دو چندان یافته است.
به گزارش مشرق به نقل از ایسنا، رضا بهرهمند، مدرس بینالمللی دورههای تربیت مربی غواصی و تکنیکال و آبهای عمیق در سلسله به تشریح بخشی از پیشرفتهای تکنیکی غواصی پرداخته است.
وی گفت: برای غواصی از تجهیزات تنفسی زیر آب استفاده می شود بدین ترتیب که غواص با همراه داشتن هوای فشرده تنفسی که درون سیلندر غواصی ذخیره شده است به زیر آب رفته و غواصی می کند. در نوعی از غواصی که به غواصی «مدار باز» موسوم است، باز دم غواص درون آب تخلیه میشود لذا غواص باید برای رسیدن به عمق زیاد سیلندرهای متعددی را با خود حمل کند. تقریبا بیشترین لوازم غواصی که در حال حاضر در اغلب مکانهای عمومی وجود دارند و مردم با آن سر و کار دارند یا میشناسند از نوع مدار باز است. این نوع سیستم اولین بار توسط Cousteau به غواصان تفریحی معرفی و عرضه شد.
برای رفع این مشکل دستگاه غواصی «مدار بسته» ابداع شده که قادر است اکسیژن موجود در بازدم غواصی را بازیابی و با ترکیبات سیلندرهای کوچک همراه ترکیب کند. با استفاده از این دستگاه نیازی به حمل سیلندرهای سنگینی متعدد نیست و غواص میتواند با تجهیزاتی به مراتب سبکتر تا سه ساعت زیرآب تنفس کند.
مدرس بینالمللی غواصی آبهای عمیق و دستگاههای مدار بسته خاطرنشان کرد: دستگاه غواصی مدار باز ذاتا ناکارآمد است چون بخش کوچکی از هر تنفسی در دستگاه متابولیسم غواصی استفاده میشود و مقدار زیادی از اکسیژن قابل استفاده دور ریخته میشود. علاوه بر این مقدار اکسیژن از دست رفته در این روش با افزایش عمق افزایش مییابد.
بهره مند تصریح کرد: دستگاه مداربسته اساسا یک دستگاه متفاوت غواصی است. سیستمهای مدار بسته تنفسی، به گونه ای ساخته شده اند که قابلیت پالایش بازدم غواص را داشته و بازدم او را با حذف دی اکسید کربن و افزودن اکسیژن برای تنفس دوباره آماده کنند. در حال حاضر سه نوع دستگاه مداربسته وجود دارد که شامل دستگاه مداربسته اکسیژن، دستگاه مداربسته نیمه بسته و دستگاه مدار بسته کامل است. این دستگاهها هر کدام دارای مزایا و معایب خاصی میباشند که به طور خلاصه به آنها می پردازیم.
وی خاطرنشان کرد: به طور کلی تمام دستگاههای مداربسته معمول اجزای مشترکی دارند. تمام آنها دارای حلقه تنفسی مجهز به یک دهنی هستند که از طریق آن غواص شروع به تنفس میکند اگر کل حلقه تنفسی (breathing loop) از جنس سفت ساخته شود غواص نمیتواند بازدم خود را دوباره به داخل برده و استنشاق کند به عبارتی مثل این است که بخواهیم در یک بطری نوشابه تنفس کنیم.
به همین علت نوعی کسیه نرم یا تاشو متصل به حلقه تنفس وجود دارد که بازدم غواص در آن میرود و آن باد میشود و وقتی نفس میکشد آن خالی میشود.به این وسیله counter lung گفته می شود که ساختاری شبیه شش یا ریه دارد.
بهره مند خاطرنشان کرد: اگر غواص در این محیط شروع به تنفس کند در مدت زمان کوتاهی CO2 بازدم آن بالا رفته و به سطح خطرناکی میرسد به همین دلیل حلقه تنفس باید وسیلهای به نام قوطی جاذب CO2 داشته باشد که حاوی نوعی مواد شیمیایی میباشد که CO2 را جذب میکند. البته جاذب CO2 به تنهایی نمیتواند به غواص کمک کند تا غواص به صورت نامحدود غواصی کند چون اکسیژن در انتها در حلقه تنفسی توسط غواص مصرف میشود پس باید توسط یک سیستم اکسیژن نیز به سیستم یا حلقه تنفس (breath loop) تزریق شود تا غواصی ادامه پیدا کند.
وی افزود: علاوه بر این، برای جلوگیری یا به عبارت دیگری پیشگیری از اینکه غواص همان هوای بازدم خود را دوباره مصرف کند، حلقه تنفسی به صورت یک طرفه و در جهت عقربههای ساعت طراحی شده است.
بدین دلیل است که upstream check valve و downstream check valve در دو طرف دهنی قرار گرفتهاند و اجازه میدهند گاز (دم) از یک طرف وارد و بازدم فقط از طرف دیگر خارج شود.
یکی دیگر از ویژگیهای مشترک بسیاری از سیستمهای تنفسی مدار بسته نحوه بستن یا shut-off کردن دهنی حلقه تنفسی است که میتوان برای جلوگیری از ورود آب به حلقه تنفسی آن را زیر آب بست و اما تفاوت اساسی میان این سه نوع از دستگاههای مدار بسته در راه اضافه نمودن گازهای مختلف به حلقه تنفسی و کنترل غلظت اکسیژن در گاز تنفسی میباشد.
بهره مند خاطرنشان کرد: دستگاه مدار بسته اکسیژن سادهترین نوع دستگاه از دستگاههای مداربسته است که نقطه شروع خوبی برای بحث در مورد دستگاههای پیچیده تر میباشد. دستگاه مدار بسته اکسیژن علاوه بر اجزای پایه ای که در ابتدا شرح داده شد، یک سیلندر اکسیژن خالص به عنوان گاز جایگزین مصرف شده توسط غواص دارد. بعضی از انواع دستگاههای مداربسته اکسیژن، اکسیژن را به میزانی ثابت که توسط خود غواص انتخاب میشود به حلقه تنفسی وارد می کند با این حال سوخت و ساز بدن با توجه به تجهیزات و پیشامدها در غواص متفاوت است. از این رو در سیستمهای Active اکسیژن خود به خود به سیستم اضافه میشود حتی هنگامی که در استراحت به سر میبریم که باعث به هدر رفتن گاز از حلقه تنفسی میباشد یا اینکه به اندازه کافی اکسیژن در هنگام کار سخت وجود ندارد که غواص به صورت دستی و نه اتوماتیک مجبور به اضافه کردن oxygen از bypass valve میشود.
وی گفت: بسیاری از دستگاههای مداربسته اکسیژن، سیستم passive addition را به دستگاه خود اضافه کردهاند که به موجب آن اکسیژن به میزان مصرف سوخت و ساز بدن غواص اضافه شده است.
یک راه ساده برای دستیابی به میزان بیشتر گاز در حال استفاده، استفاده کردن از شیر مکانیکی میباشد که گاز را به counter lung اضافه میکند، از این روش در هنگامی که counter lung کاملا از کار میافتد نیز استفاده میشود. بدین ترتیب که بدن غواص، اکسیژن را گرفته و دی اکسید کربن تولید میکند. دی اکسید کربن توسط جاذب حذف شده و حجم گاز در حلقه تنفسی کاهش پیدا میکند، در نهایت مکیدن کامل هوا از دهان باعث بسته شدن counter lung میشود و در این زمان باید به روش مانوآل و دستی توسط شیر مکانیکی به اکسیژن اضافه کرد.
بهره مند تصریح کرد: در این سیستم بسیار مهم و حیاتی است که هنگام شروع غواصی اکسیژن خالص را وارد حلقه تنفسی کنیم. اگر حجم زیادی از گازهای دیگر در حلقه تنفسی وجود داشته باشد، ممکن است غواص قبل از فعال شدن شیر مکانیکی دچار hypoxia شود. چرا که پتانسیل برای مسمومیت اکسیژن بسیار زیاد است.
مسمومیت اکسیژن (CNS) در اعماق بیشتر از شش متر یا 40 فوت به وجود میآید و مانع از بهرهبرداری بیشتر توسط این نوع دستگاه میشود و برای دستیابی به عمقهای بیشتر باید از مخلوط گازهای دیگر (نیتروژن، هلیوم) استفاده کرد که مستلزم به کارگیری دستگاههای نیمه مداربسته یا مداربسته کامل است.
دستگاه نیمه مداربسته برخلاف دستگاه مدار بسته اکسیژن، دارای فرمهای گاز مخلوط مداربسته میباشد که در آن گازهای دیگری به غیر از اکسیژن خالص در نظر گرفته شده است.
فرمول شیمیایی آب
آب نوعی ماده مرکب است که از دو عنصر اکسیژن و هیدروژن ساخته شده است. آب را جزو دسته مخلوطها طبقهبندی نمیکنند، چون خواص آب نه به خواص هیدروژن شبیه است و نه به خواص اکسیژن. از ترکیب دو اتم هیدروژن و یک اتم اکسیژن، یک مولکول آب بوجود میآید. یک قطره آب دارای تعداد بی شماری مولکول آب میباشد.معادله شیمیایی واکنش بین هیدروژن و اکسیژن و تشکیل آب از قرار زیر است:
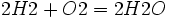
هر مولکول آب دارای یک ناحیه مثبت و یک ناحیه منفی است که این دو ناحیه در دو طرف مولکول آب واقع شدهاند. شیمیدانها با کمک شواهد به این نتیجه رسیدهاند که مولکول آب شکل خطی ندارد، یعنی به این صورت نیست که دو اتم هیدروژن بصورت خطی در دو طرف یک اتم اکسیژن قرار گرفته باشند (HــOــH). بلکه مولکول آب حالت خمیده ای دارد که اتم های هیدروژن در سر مثبت مولکول و اتم های اکسیژن در سر منفی مولکول آب تجمع پیدا نموده اند.
طبقه بندی قدرت نسبی اسیدها و بازها
بهترین راه برای مشاهده قدرت نسبی اسیدهای ضعیف از نظر کمی، به کارگیری جدول ثابت تفکیک اسیدی است، ولی شما غالباً با مشاهده فرمول آنها، می توانید به طور کیفی ضعیف یا قوی بودن اسید را طبقه بندی کنید.
اسیدهای قوی: دو نوع اسید قوی و مثال های مربوط به آنها عبارتند از:
1- هیدروهالیک اسیدها (اسیدهای بدون اکسیژن)، HI ، HBr ، HCl
2- اکسواسیدها (اسیدهای اکسیژن دار) که در آنها تعداد اتم اکسیژن دو یا بیشتر، بیش از تعداد پروتون های قابل یونش (هیدروژن های اسیدی) می باشد. (اختلاف تعداد اکسیژن و هیدروژن 2 و یا 3 است). این اسیدها مانند HNO3 ، H2SO4 و HClO4 می باشند، برای مثال در H2SO4 تعداد هیدروژن ها 2 و تعداد اکسیژن ها 4 است، یعنی تعداد اکسیژن دو تا بیشتر از تعداد هیدروژن 2 = 2 - 4
اسیدهای ضعیف: تعداد اسیدهای ضعیف بیشتر از اسیدهای قوی است. چهار نوع از این اسیدها با مثال مربوطه عبارتند از:
1- هیدروهالیک اسید HF
2- اسیدهایی که در ساختار آنها، H به O یا هالوژن متصل نیست مانند HCN و H2S
3- اکسو اسیدهایی که تعداد اتم های O مساوی و یا یکی بیشتر از تعداد هیدروژن های قابل یونش هستند، (اختلاف اکسیژن و هیدروژن صفر و یا یک است) مانند HClO ، HNO2 ، H3PO4
4- کربوکسیلیک اسیدها (فرمول کلی RCOOH که پروتون های قابل یونش در آنها به اکسیژن متصل است. مانند CH3COOH ، C6H5COOH
بازهای قوی: ترکیب های محلول در آب که یون های اکسید (O2- ) یا هیدروکسید (OH-) دارند. بازهای قوی هستند. کاتیون این بازها معمولاً از فلزهای فعال هستند.
1- M2O یا MOH که M فلز گروه 1 (IA) مانند Cs , Rb , K , Na , Li است.
2- MO یا M(OH)2 که M فلز گروه 2 (IIA) مانند Ba , Sr , Ca می باشد.
( MgO و Mg(OH)2 فقط کمی در آب حل می شوند و مقدار حل شده آن در آب به طور کامل تفکیک می شود.)
بازهای ضعیف: بسیاری از ترکیب ها با نیتروژن غنی از الکترون (دارای جفت الکترون آزاد) بازهای ضعیف هستند. (طبق تعریف آرنیوس باز محسوب نمی شوند) ساختار متداول اتم یک نیتروژن با زوج الکترون آزاد است.
1- آمونیاک ( NH3)
2- آمین ها (فرمول عمومی RNH2 ، R2NH یا R3N ) مانند CH3CH2NH2 ، (CH3)2NH و CH3)3N)
انتشار یافته در وبلاگ دهکده - آموزش شیمی
منبع: اصول شیمی عمومی سیلبربرگ، ترجمه دکتر مجید میرمحمد صادقی، دکتر غلامعباس پارسافر، دکتر محمدرضا سعیدی